徐媛, 刘宝, 牛玉林, 晁晟, 张涛, 杨麒臻, 潘光辉, 李海洋
(1.贵州医科大学附属医院 器官移植中心,贵州 贵阳 550004; 2.贵州医科大学附属医院 检验科,贵州 贵阳 550004)
肾移植(kidney transplant,KT)术后患者免疫力低下、感染发病率高,其中耐药菌感染是影响术后患者预后的重要因素[1],一些特殊耐药菌感染与患者术后早期死亡率有显着相关性[2]。KT患者不同耐药菌感染的危险因素不同,发生感染后对抗生素的耐药性反应也有差异[3-4]。与非耐药病原体感染相比,耐药细菌引起的感染、复发性感染以及同种异体移植物功能障碍更为显着,死亡率上升的风险增加[5]。泌尿系、肺部等不同部位的感染,致病菌的菌株和耐药性差异较大,但目前国内相关研究结果不完全一致,具有较明显的地区差异性[6-7]。因此分析本地区KT人群的易感因素,并对不同感染部位的耐药菌分布构成进行分析,具有一定临床意义。本研究收集行同种异体KT术的196例患者的相关资料,对感染部位、取病原体阳性培养结果的病原学种类及其耐药率进行分析,以期为KT术后感染患者合理使用抗生素提供参考。
1 对象与方法
1.1 研究对象
选择2017年4月—2019年3月行同种异体KT术患者196例,术前根据人白细胞抗原配型相合位点及群体反应性抗体情况给予两联(复宁+甲泼尼龙方案)或三联(复宁+舒莱+甲泼尼龙)免疫诱导,术后常规予他克莫司+吗替麦考酚酯+甲泼尼龙口服抗排异治疗;术前常规送检肾脏灌洗液、供肾血管组织,术后取痰、尿、引流液以及伤口分泌物进行细菌培养和真菌培养,记录患者术后12月内发生感染的部位、病原学培养及耐药(耐药率)情况。纳入标准:(1)行KT手术时留取了供肾血管组织、肾脏灌洗液、尿液、静脉血标本的患者,对术后疑似感染的患者加做粪便培养;(2)术后随访过程中,临床疑似感染而留取引流液、血液、痰液、尿液、粪便标本的KT患者;(3)病历资料完善。排除临床疑似、缺乏微生物室检查样本送检的KT患者。收集患者性别、年龄、透析时间、诱导方案、术后是否发生排斥反应及移植肾功能延迟恢复等资料,同时对感染部位、取得阳性培养结果的病原学种类及其耐药率进行分析。共纳入KT术后随访观察期内取得阳性培养结果的患者72名,感染率36.73%;共送检各类标本1 792例次(去除同一患者同一相同部位培养出的相同病原体药敏结果),共检出阳性结果127例次(7.09%),其中细菌感染占比82.68%。术后因出血行移植肾切除1例,严重肺部感染死亡1例,术后1年人肾存活率为99.49%。
1.2 研究方法
1.2.1主要试剂与仪器 BD血培养瓶和FX200全自动血培养仪(美国,BD公司)、BACTEC(TM)、Walk Away 96 型全自动细菌鉴定仪(德国,西门子公司)、西门子革兰氏阳性菌鉴定及药敏板(产品编号B1017-211)、革兰阴性菌鉴定及药敏板(产品编号B1017-414)。
1.2.2观察指标 记录感染患者的感染好发部位、对留存送检标本行细菌培养,采用全自动微生物鉴定仪分离鉴定病原菌类型,对病原分离株进行药物敏感试验,采用WHONET5. 6软件对药敏结果进行分析,按照美国实验室标准化协会CLSI2015版标准进行结果判定,记录病原菌种类以及耐药情况。
2 结果
2.1 病原菌来源及构成比
KT术后感染发病率为36.73%(72/196),尿路感染(45/127)和以供肾血管组织、灌洗液阳性表现的供体来源感染(38/127)是最常见的感染部位。72例KT术后患者感染患者共分离出病原菌127株,其中革兰阴性杆菌76株、革兰阳性球菌42株、真菌9株;排名前3的革兰阴性杆菌分别为大肠埃希菌(22株)、肺炎克雷伯菌(13株)、鲍曼不动杆菌(9株);排名前3的革兰阳性球菌分别为屎肠球菌(17株)、表皮葡萄球菌(8株)、溶血葡萄球菌(6株);真菌培养阳性者均为假丝酵母菌属的白假丝酵母菌(9株)。见表1。
2.2 KT术后革兰阴性杆菌的药敏结果
KT术后革兰阴性杆菌多为多重耐药或泛耐药菌群,其中嗜麦芽黄单胞菌、大肠埃希菌和鲍曼不动杆菌的耐药率最高。抗生素中头孢西丁钠、头孢唑林钠、氨苄西林以及厄他培南等在多个菌群中耐药率高达100%。见表2。
2.3 KT术后革兰阳性球菌药敏结果
KT术后患者分离革兰阳性球菌耐药率最高的是溶血葡萄球菌,所有革兰阳性球菌均对抗生素万古霉素和利奈唑胺敏感。抗生素中达托霉素、呋喃妥因及喹奴普丁/达福普汀的耐药率较低。见表3。
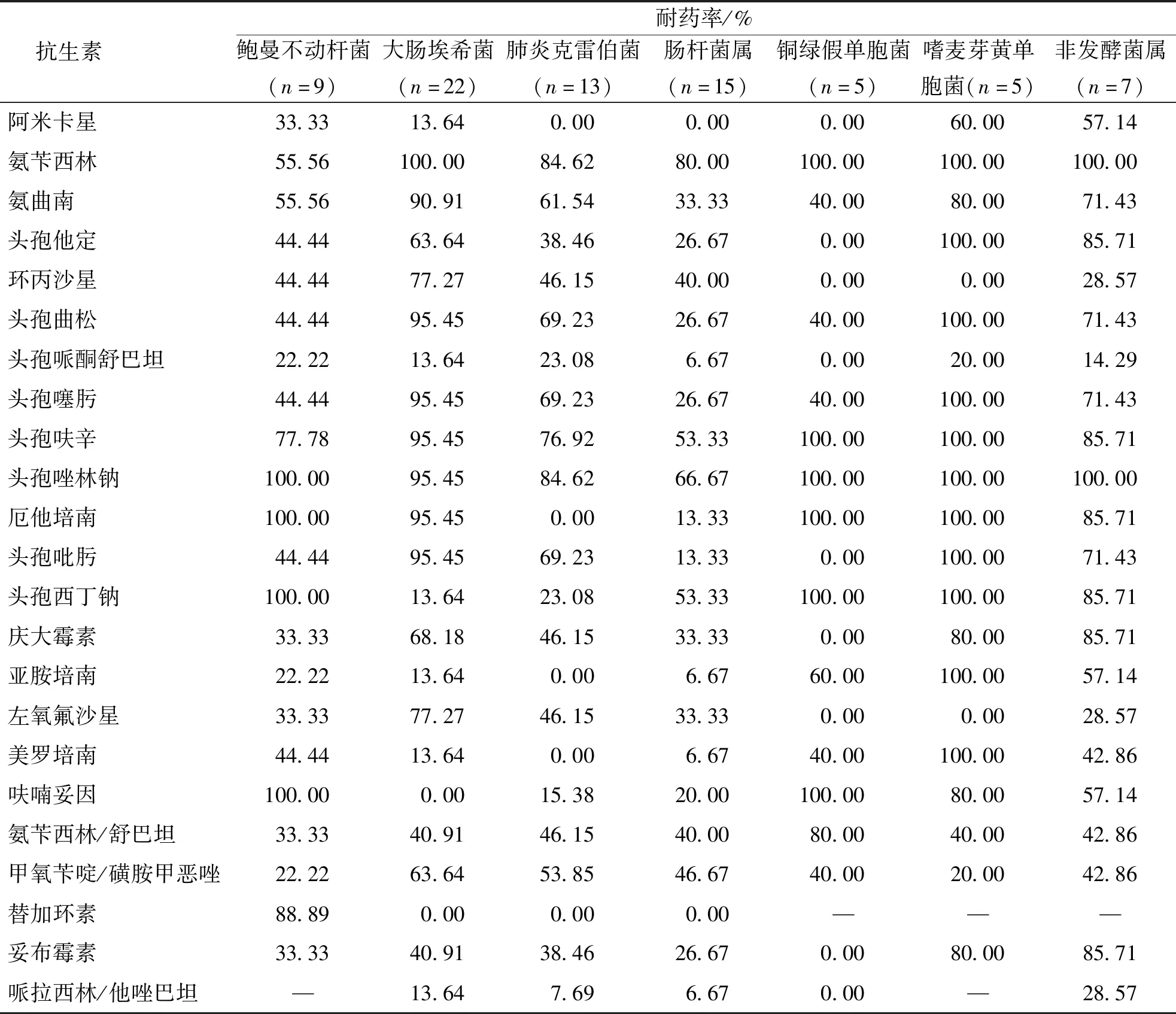
表2 KT术后感染患者检出革兰阴性杆菌的药敏实验结果Tab.2 Drug resistance rate of Gram-bacillus infection in KT patients
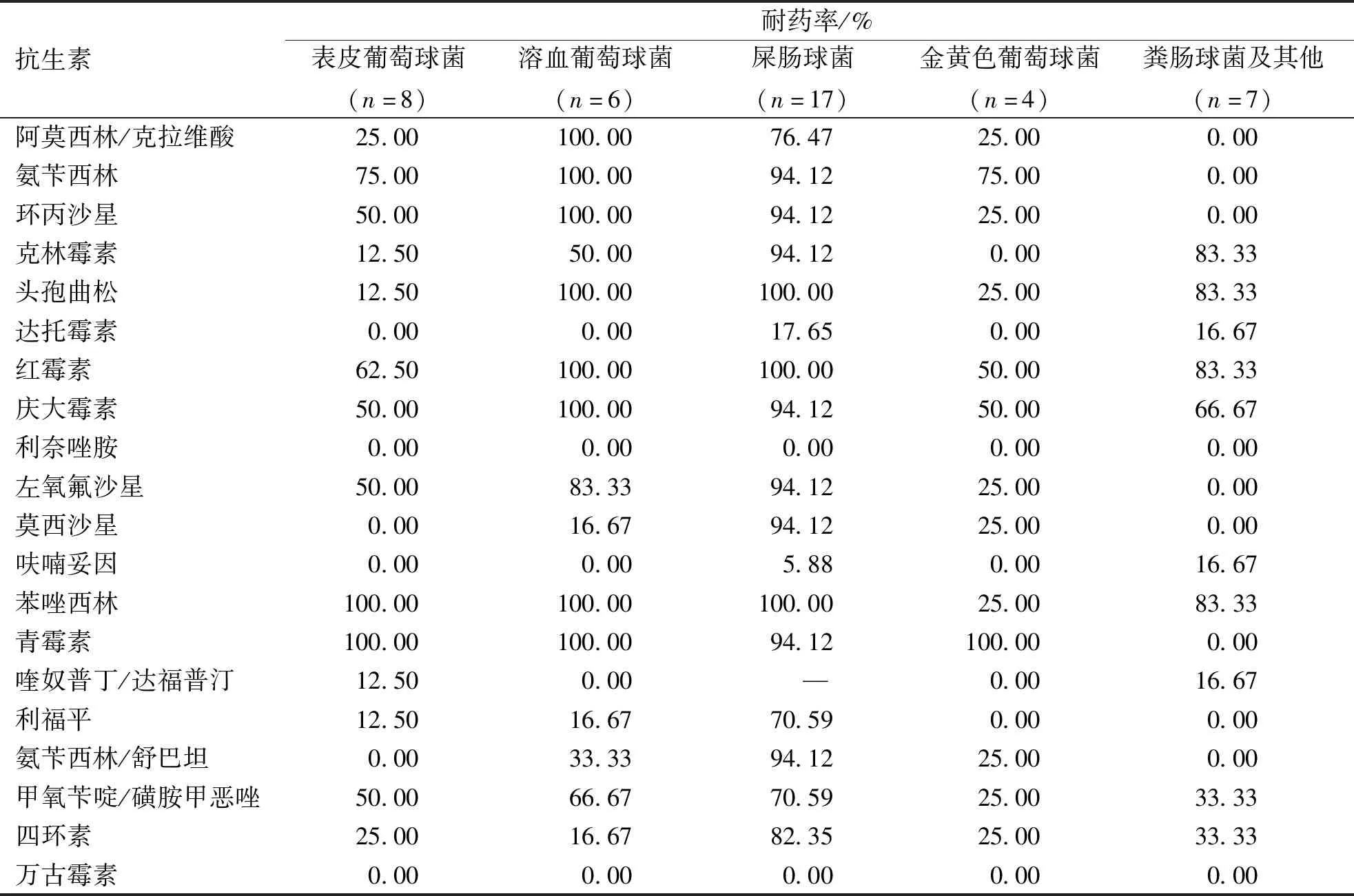
表3 KT患者感染的革兰阳性球菌耐药率/%Tab.3 Drug resistance rate of Gram-positive cocci infection in kidney transplant patients/%
3 讨论
KT患者术后早期容易发生感染的主要因素有:(1)长期留置血液透析管或腹膜透析管,易造成血源性腹腔或腹腔感染;(2)尿毒症患者社区获得性肺炎的发生率增加;(3)术前术后免疫诱导剂免疫抑制剂的使用;(4)DCD供体使用呼吸机等侵入性操作及重症监护室环境等因素,也增加了耐药菌株的感染风险[8-9]。
本研究显示,在术后早期KT患者发生感染的病原菌培养来源中,供肾组织或灌洗液/引流液的培养阳性菌株38例,占比高达29%,供体来源的感染正成为KT手术病人的重要感染来源之一。这与国内外同类型研究相符[10-12],提示加强供体的术前筛查与术后早期预防性应用抗生素必不可少。感染来源中最多的是清洁中段尿培养,培养结果多为多重耐药的肺炎克雷伯菌,此类尿路感染可能增加患者的病死率,尤其应该得到重视[13]。在移植术后早期的多重耐药菌感染中,最令人担忧的是供者来源的耐碳青霉烯类肺炎克雷伯菌(carbapenem-resistantKlebsiellapneumoniae,CRKP)感染,此类感染易引起移植肾动脉炎、假性动脉瘤形成,甚至发生动脉瘤破裂大出血危及受者生命[14]。值得一提的是,供体来源的CRKP感染在此次单中心的药敏实验中多呈泛耐药或全耐药状态,对美罗培南和替加环素不敏感。本中心过去4例培养出全耐药CRKP的KT患者中,均给予头孢他定-阿维巴坦后治愈。本研究发现,肾脏移植患者细菌性肺炎是肺部感染的最常见原因,早期最常见的病原体是革兰阴性杆菌(肺炎克雷伯菌,大肠埃希菌,铜绿假单胞菌等),但革兰阳性球菌如金黄色葡萄球菌或肺炎链球菌和厌氧菌也可发现。移植后6个月,肺炎主要归因于社区获得性细菌(肺炎链球菌、流感嗜血杆菌、支原体及衣原体等)[15-16]。本研究196例患者中,术后早期(移植后12月内)临床诊断为肺部感染的49人,通过痰培养明确病原菌的患者19人,痰培养结果阳性率38.78%。部分病人由于病情无法留取痰液或肺泡灌洗液。器官移植术后患者肺部感染病原学多样,除一般细菌感染外,耶氏肺孢子虫、巨细胞病毒、霉菌感染也较为常见,此类重症肺炎在治疗后期易合并多重耐药菌的感染[17-19]。类似美罗培南、万古霉素等广谱抗菌药物的长期过度使用,有增加患者多重耐药细菌感染的风险,同时也容易引起机体菌群失调导致继发的侵袭性真菌肺部感染的可能[20]。近年来基于宏基因组学的二代测序技术(mNGS)已逐渐成熟,有益于提供临床上查找感染的病原学依据。通过对患者的血液、痰液以及肺泡灌洗液的检测,能够提高病原学监测的阳性率及临床采信率,降低感染患者的28 d病死率[21]。因此,在未来的样本筛查中选择性地开展mNGS技术,将有助于早期明确KT术后患者的感染源,提供对细菌、真菌、和病毒的治疗依据。免疫抑制和免疫耐受机制在侵袭性真菌感染治疗反应中的作用是器官移植人群中的重要因素,抗真菌药的选择不仅应考虑其毒性,还应考虑其对免疫系统的影响[22]。
综上所述,KT术后患者的早期感染率较高,且感染病原菌的耐药率较高[23],本研究提示早期开展病原学监测、合理选用抗生素是提高患者治愈率及减少耐药菌群传播的有效手段。



