周福林,宋少飞,弓巧娟,张稳婵,周 蓓
(运城学院应用化学系,山西 运城 044000)
催化氧化荧光法测定防腐剂苯甲酸
周福林,宋少飞,弓巧娟,张稳婵,周 蓓
(运城学院应用化学系,山西 运城 044000)
在pH8的NaH2PO4-Na2HPO4缓冲溶液中,Co2+催化KBrO3氧化苯甲酸产生强荧光,建立催化氧化荧光法间接测定苯甲酸的新方法。在最优化条件下,苯甲酸质量浓度在5×10-7~3×10-5g/mL范围内与荧光强度呈良好的线性关系,方法的检出限为2×10-8g/mL。对质量浓度为1×10-6g/mL的苯甲酸标准溶液进行11次平行测定,得相对标准偏差(RSD)为1.9%。该法应用于食醋及酱油中苯甲酸的测定,回收率为95.7%~101.6%,结果令人满意。
催化氧化;荧光法;苯甲酸;防腐剂
Abstract:Based on the catalytic effect of cobalt (II) on the oxidation of benzoic acid by potassium bromate in NaH2PO4-Na2HPO4 buffer solution at the condition of pH 8, a new catalytic oxidation fluorometry method was proposed for the indirect determination of benzoic acid. Under optimal determination conditions, an excellent linear relationship between benzoic acid concentration within a range of 5×10-7-3×10-5g/mL and fluorescence intensity was observed. The detection limit of this established method was 2×10-8g/mL. The reproducibility experiments revealed the relative standard deviation (RSD) of 1.9%for benzoic acid solution at the concentration of 1×10-6g/mL. This established method has been applied for the detection of benzoic acid in vinegar and sauce. The recovery rates were in the range of 95.7%-101.6% with satisfactory results.
Key words:catalysis oxidation;fluorimetry;benzoic acid;preservative
苯甲酸又名安息香酸(C6H5COOH)是一种有机化学防腐剂,具有杀死或抑制细菌生长和繁殖的作用,被广泛应用于食品工业。但是超标准使用防腐剂会加重人的肝脏负担并引起毒性反应,严重损害人体健康。我国对防腐剂使用有着严格的规定[1],酱油和食醋是人们日常饮食中广泛使用的调味剂,因此测定酱油和食醋中的苯甲酸具有十分重要的意义。
目前,国内外对苯甲酸的测定方法主要有高效液相色谱法[2-7]、气相色谱法[8-11]和紫外光度法[12-14],此外,还有毛细管电泳法[15-16]、离子色谱法[17]、极谱法[18]、化学发光法[19]等。催化动力学荧光法具有仪器简单、灵敏度高、检出限低等优点,用此法研究苯甲酸的报道目前甚少[20]。本实验在酸性条件下,Co2+催化KBrO3氧化苯甲酸产生强荧光,建立测定苯甲酸的催化氧化荧光新方法。
1 材料与方法
1.1 材料、试剂与仪器
酱油 佛山市海天调味食品有限公司;白醋 太原市古灯调味食品有限公司。
1×10-2g/mL苯甲酸标准溶液,临用时逐级稀释;NaH2PO4-Na2HPO4缓冲溶液pH8;0.25mol/L KBrO3溶液、3.125×10-2mol/L Co(NO3)2溶液。实验所用水均为二次蒸馏水,所用试剂均为分析纯。
F-4600 荧光分光光度计 日本日立公司;FA1104型电子天平 上海恒平科学仪器有限公司;HHS型电热恒温水浴锅 天津市华北实验仪器有限公司。
1.2 方法
在两支25mL比色管中,一支加入一定量的苯甲酸标准溶液,另一支不加(空白),再分别准确加入2mL NaH2PO4-Na2HPO4缓冲溶液,3mL KBrO3溶液,0.8mLCo(NO3)2溶液,用二次蒸馏水稀释至刻度,摇匀。在40℃的水浴中加热18min,冷水冷却后,以303nm为激发波长,602nm为发射波长分别测定它们的荧光强度,催化反应荧光强度为I,非催化反应荧光强度为I0,计算ΔI=I-I0。
2 结果与分析
2.1 激发和发射光谱
配制不同体系的溶液(图1),用荧光分光光度计分别绘制激发和发射光谱。图1曲线1、1′是苯甲酸溶液的荧光光谱,曲线2、2′说明KBrO3能氧化苯甲酸发出强荧光,当体系中加入Co(NO3)2后,反应速率明显加快(曲线3、3′),而且只增强了荧光强度,光谱形状并没有改变,说明Co2+对此反应有明显的催化作用。
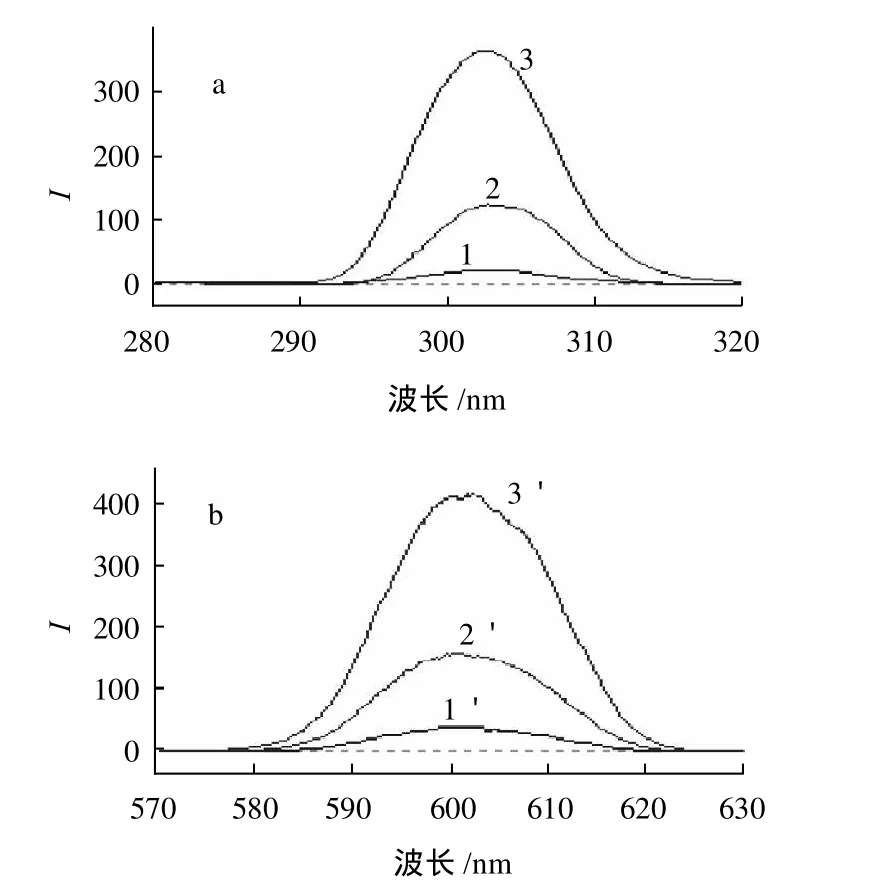
图1 荧光激发(a)和发射(b)光谱Fig.1 Excitation and emission spectra of reaction system
2.2 反应条件的选择
2.2.1 波长的选择
由图1可见,几种体系溶液的最大激发波长和最大发射波长均在303nm和602nm处。因此,本实验选最大激发波长和最大发射波长分别为303nm和602nm。
2.2.2 缓冲溶液体积的影响
溶液酸度是影响反应的重要参数之一。本实验选择磷酸盐作为缓冲溶液,发现pH8时,荧光强度最大,故实验选用pH8的NaH2PO4-Na2HPO4缓冲溶液。实验对缓冲溶液体积进行了考察。如图2所示,当缓冲溶液的体积为2.0mL时,ΔI最大,固实验选择pH8的NaH2PO4-Na2HPO4缓冲溶液的体积为2.0mL。
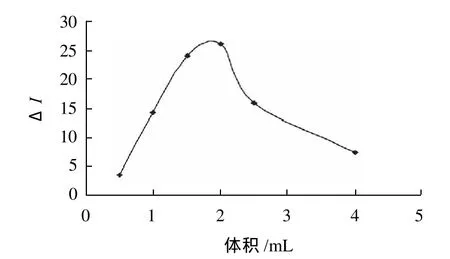
图2 缓冲溶液体积的影响Fig.2 Effect of buffer solution volume on fluorescence intensity
2.2.3 KBrO3浓度的影响
实验考察0.005~0.035mol/L范围内不同浓度KBrO3对荧光强度的影响(图3)。当KBrO3浓度为0.03mol/L时,ΔI最大。因此,本实验选择KBrO3溶液的最佳浓度为0.03mol/L。
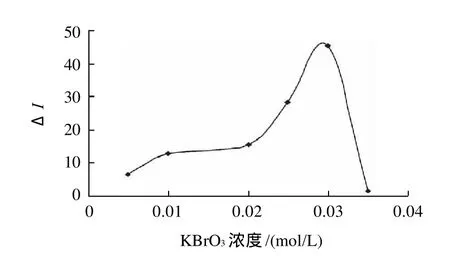
图3 KBrO3浓度的影响Fig.3 Effect of KBrO3concentration on fluorescence intensity
2.2.4 Co(NO3)2浓度的影响
由图4可见,随着Co(NO3)2浓度的增大,ΔI也增大,当Co(NO3)2浓度大于1.0×10-3mol/L时,ΔI反而降低。所以Co(NO3)2溶液的最佳浓度为1×10-3mol/L。
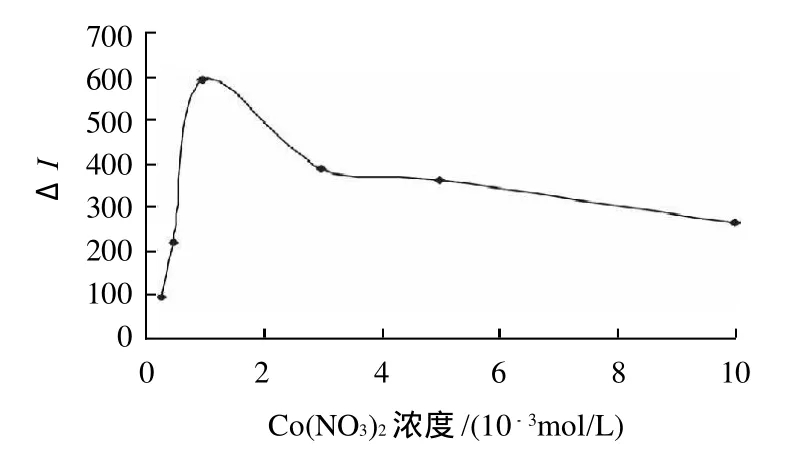
图4 Co(NO3)2浓度的影响Fig.4 Effect of Co(NO3)2concentration on fluorescence intensity
2.2.5 反应温度的影响
实验对反应温度进行考察,结果表明(图5),当温度为40℃时,ΔI达到最大值,所以最佳反应温度为40℃。
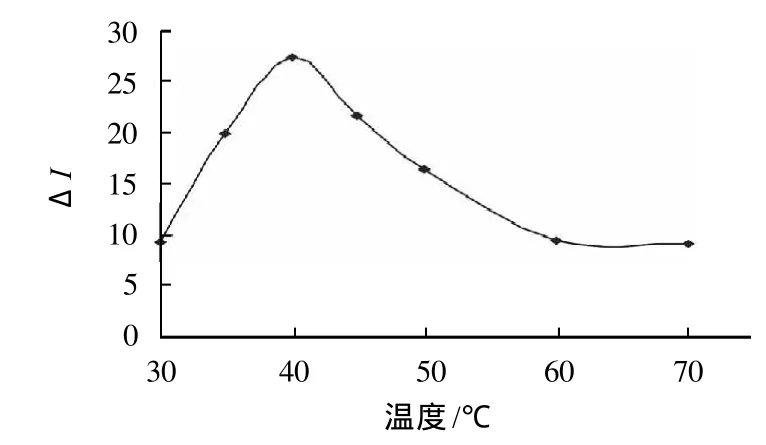
图5 反应温度的影响Fig.5 Effect of reaction temperature on fluorescence intensity
2.2.6 反应时间的影响
ΔI值随着反应时间的增加而增大,当时间大于18min时,ΔI值随着时间的增加反而减小(图6)。所以,本实验选择的反应时间为18min。

图6 反应时间的影响Fig.6 Effect of reaction time on fluorescence intensity
2.3 苯甲酸标准曲线的绘制
按上述实验方法,在最优实验条件下,对不同质量浓度的苯甲酸标准溶液进行测定。苯甲酸质量浓度在5×10-7~3×10-5g/mL范围内与ΔI成线性关系(图7),其回归方程为ΔI=40.85C+792.6(C为标准品质量浓度/(10-6g/mL)),r=0.9979。
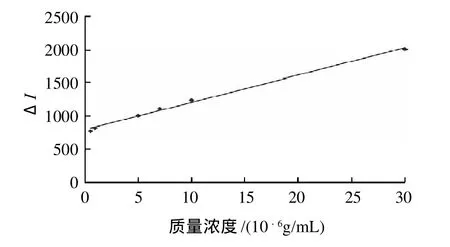
图7 苯甲酸标准曲线Fig.7 Standard curve establishment for the determination of benzoic acid
2.4 精密度与检出限
按实验方法,对质量浓度为1×10-6g/mL的苯甲酸标准溶液进行11次平行测定,相对标准偏差为1.9%,根据IUPAC建议,计算出该方法的检出限是2×10-8g/mL。
2.5 共存离子的影响
实验考察不同物质对苯甲酸的干扰实验,对相同质量浓度的苯甲酸(1×10-6g/mL),测量误差在±5%以内,结果如下:Na+、K+、Ag+、BrO3-(1000 倍),Mg2+、Ca2+、Zn2+、Cd2+、NO3-、Cl-(500 倍),PO43-、Al3+、Cr3+(400倍),SO42-(350倍)不干扰测定。
2.6 样品分析
实验对酱油和白醋中的苯甲酸进行了测定,取酱油和白醋各1mL,稀释至50mL,分别取稀释后的样品溶液1、2、3mL,按2.2节实验方法进行测定,同时进行了加标回收实验,结果见表1。

表1 酱油和白醋中苯甲酸的测定结果(n=6)Table l Determination of benzoic acid in sauce and white vinegar (n=6)
2.7 反应机理研究
在pH8的NaH2PO4-Na2HPO4缓冲溶液介质中,40℃水浴条件下,KBrO3氧化苯甲酸发出强荧光。反应进行的较慢,当体系中加入Co2+后,反应速率明显加快,荧光强度得到了增强,但光谱形状没有改变,可以认为Co2+在此体系中起催化作用。根据有关文献机理的探讨和该催化反应体系的荧光光谱行为[21-22],推测催化反应机理如下:

图8 苯甲酸催化反应机理Fig.8 Catalytic reaction mechanism of benzoic acid
3 结 论
本实验建立了间接测定苯甲酸的催化氧化荧光新方法,该方法具有灵敏度高,选择性好,操作简便等优点。已用于食醋及酱油中苯甲酸的测定,回收率为95.7%~101.6%,结果令人满意。
[1] GB 2760—1996 食品添加剂使用卫生标准[S].
[2] MIHYAR G F, YOUSIF A K, YAMANI M I. Determination of benzoic and sorbic acids in labaneh by high-performance liquid chromatography[J]. J Food Compos Anal, 1999, 12:53-61.
[3] TFOUNI S A V, TOLEDO M C F. Determination of benzoic and sorbic acids in brazilian food[J]. Food Control, 2002, 13:117-123.
[4] KOYUNCU N, UYLA ER V. Determination of benzoic and sorbic acid in turkish food using high-performance liquid chromatography[J]. J Food Process Preserv, 2009, 33:361-369.
[5] 宋文青, 刘亚雄, 王琴, 等. 无筛板型固相萃取柱的制备及其在食品中苯甲酸的测定研究[J]. 分析化学, 2009, 37(10):1507-1510.
[6] 陈昌云, 丁爱芳, 赵波, 等. 固相萃取-高效液相色谱法测定肉制品中山梨酸、苯甲酸含量[J]. 食品科学, 2009, 30(18):344-346.
[7] 鄢盛华. 分散固相萃取高效液相色谱法测定酱油中苯甲酸和山梨酸[J]. 理化检验:化学分册, 2009, 45(8):1006-1007.
[8] PAN Zaifa, WANG Lili, MO Weiming, et al. Determination of benzoic acid in soft drinks by gas chromatography with on-line pyrolytic methylation technique[J]. Anal Chim Acta, 2005, 545:218-223.
[9] 董长波. 大口径毛细管气相色谱法测定酱油中山梨酸、苯甲酸方法研究[J]. 中国卫生检验杂志, 2009, 19(3):567-568.
[10] 张媛媛, 寇登民, 张静, 等. 对甲苯磺酸三乙铵作为气相色谱固定相测定酱油中的苯甲酸[J]. 分析测试学报, 2006, 25(2):115-116; 119.
[11] 甘平胜, 黄聪, 于鸿, 等. 气相色谱-质谱联用法测定奶粉中苯甲酸(钠)含量[J]. 中国卫生检验杂志, 2008, 18(1):75-76.
[12] 于晓萍. 紫外分光光度法快速测定蜜饯中苯甲酸的含量[J]. 化学工业与工程技术, 2009, 30(3):42-44.
[13] 暴玮, 刘雄民, 马丽, 等. 紫外分光光度法测定肉桂醛、苯甲醛和苯甲酸[J]. 理化检验:化学分册, 2009, 45(6):687-689; 694.
[14] 付俊, 代加林, 王鹤, 等. 支持向量回归-分光光度法对苯酚、苯胺和苯甲酸的同时测定[J]. 分析试验室, 2009, 28(10):95-98.
[15] HAN Fang, HE Youzhao, LI Lian, et al. Determination of benzoic acid and sorbic acid in food products using electrokinetic flow analysis-ion pair solid phase extraction-capillary zone electrophoresis[J]. Anal Chim Acta, 2008, 618:79-85.
[16] 衷明华, 李云. 毛细管电泳法分离测定潮汕凉果中的山梨酸、苯甲酸、糖精钠[J]. 光谱实验室, 2009, 26(6):1568-1571.
[17] 刘巧茹, 褚松茂, 杨维春, 等. 高效离子色谱法测定辣椒红色素中苯甲酸含量[J]. 食品科学, 2009, 30(12):180-182.
[18] 金华丽, 李漫男, 赵端阳. 示波极谱法测定食品中苯甲酸的研究[J].食品工业科技, 2009, 30(6):346-347; 391.
[19] 张虹蔚, 高旭晖, 常旭红, 等. 流动注射化学发光测定苯甲酸[J]. 福州大学学报:自然科学版, 1999, 27:27-28.
[20] 魏敏, 瞿鹏, 李国防, 等. 催化动力学荧光法测定酱油中的苯甲酸[J].商丘师范学院学报, 2007, 23(9):68-70.
[21] DUMA V, POPP K E, KUNG M C, et al. Gas phase oxidation of benzoic acid to phenol over nickel oxide catalysts[J]. Chem Eng J, 2004,99(3):227-236.
[22] SCHNECK C M, PONCHERI A J, JENNINGS J T, et al. Competition between solvent quenching and indole quenching of 9-fluorenone:a spectroscopic and computational study[J]. Spectrochim Acta:Part A,2010, 75(2):624-628.
Determination of Preservative Benzoic Acid by Catalytic Oxidation Fluorometry
ZHOU Fu-lin,SONG Shao-fei,GONG Qiao-juan,ZHANG Wen-chan,ZHOU Bei
(Department of Applied Chemistry, Yuncheng University, Yuncheng 044000, China)
O657. 32
A
1002-6630(2010)22-0417-04
2010-02-06
运城学院2009年度院级基础研究项目(JC-2009005);运城学院基金项目(20060228);山西省教育厅高等教育研究基金项目(200713033)
周福林(1980—),女,讲师,硕士,主要从事仪器分析及食品分析的应用研究。E-mail:ssfzfl@163.com



