蒋 芸,严文静,刘丽强,匡 华,陈 伟,张 坤,胥传来,*
(1.苏州大学分析测试中心,江苏 苏州 215123;2.江南大学食品学院,江苏 无锡 214122)
重金属汞螯合物人工抗原的合成与鉴定
蒋 芸1,严文静2,刘丽强2,匡 华2,陈 伟2,张 坤2,胥传来2,*
(1.苏州大学分析测试中心,江苏 苏州 215123;2.江南大学食品学院,江苏 无锡 214122)
以重金属汞为起始物质,将其离子化为二价汞,与双功能螯合剂谷胱甘肽(GSH)螯合后,获得半抗原,然后将半抗原与载体蛋白牛血清白蛋白(BSA)、卵清蛋白(OVA)进行偶联,获得完全抗原。实验对各步骤的反应条件进行优化,采用紫外光谱、凝胶电泳对产物进行表征,成功制备了汞-GSH-BSA完全抗原。为计算完全抗原中重金属和载体蛋白的偶联比,采用石墨炉原子吸收法测定产物中重金属汞的含量,采用二喹啉甲酸(BCA)法测定抗原中载体蛋白的含量,所制备的免疫原中汞和蛋白的偶联比是9:1。Hg-GSH-BSA的成功合成是制备可识别重金属汞螯合物抗体的基础。
汞;重金属;免疫学检测;双功能螯合剂;抗原
重金属污染给生态环境和人类健康带来严重的危害,特别是汞,因其环境行为的复杂性和毒性,引起了广泛关注[1-4]。汞及其化合物所造成的生态污染问题日益严重,汞沿着食物链的累积,可以通过多种途径进入人体,对人的呼吸系统、皮肤、中枢神经系统、肾脏和眼睛等造成严重伤害[5-8]。重金属免疫学检测技术具有检测速度快、费用低廉、灵敏度高和选择性强等优点,可用于环境样品重金属筛查、农畜产品的抽样检测及进出口通关的快速检验中。重金属免疫检测技术以重金属螯合物特异性单克隆抗体为基础,而成功制备重金属免疫原是制备单克隆抗体的关键[9-14]。
1 材料与方法
1.1 材料与试剂
汞、牛血清蛋白、钥孔戚血蓝素(KLH)、卵清蛋白(OVA) 美国Sigma公司;乙二胺四乙酸(EDTA) 北京精益化工厂;二乙烯三胺五乙酸(DTPA) 上海同仁化学研究所;羟乙基哌嗪乙磺酸(HEPES) 华美生物工程公司; BCA蛋白质检测试剂盒 德国Merck公司;Milli-Q超纯水 美国Millipore公司。
1.2 仪器与设备
自动高速冷冻离心机 日立(上海)仪器有限公司;赛多利斯arium 611UF实验室超纯水器 赛多利斯科学仪器(北京)有限公司;UV2V IS8500型分光光度计 Unico(上海)仪器有限公司;ENWAY 3520 pH计 基因有限公司;Power PAC3000型电泳仪 美国Bio-Rad公司;DYCZ-24DN(小号) 双垂直电泳槽 东莞市麦亘生物科技有限公司;IKA磁力搅拌器 广州仪科实验室技术有限公司。
1.3 方法
1.3.1 完全抗原的制备
取10mg 金属汞,溶于5mL 浓硝酸中,待其完全溶解后补加超纯水至50mL,调制成1mmol/L 的Hg2+溶液待用。
采用水溶性碳化二亚胺(EDC)偶联牛血清白蛋白(BSA)与谷胱甘肽(GSH)。用去离子水分别配制5mg/mL的GSH、0.5%的EDC。BSA 20mg溶于1.4mL pH7.4的HEPES (10mmol/L)缓冲液中,取0.6mL质量浓度为5mg/mL的GSH逐滴滴加到1.4mL的BSA中,再加入2mL 0.5% EDC,25℃反应8h,调节pH值至7.4,25℃反应4h。
反应物纯化后加入50μL的lmmol/L的Hg2+溶液,25℃反应6h。用磁力搅拌器对反应液进行透析,透析3d,小分子物质被滤去。即形成完全抗原BSAGSH-Hg2+。
1.3.2 无金属抗原BSA-GSH的制备
用去离子水分别配制5mg/mL的GSH、0.5%的EDC。BSA 20mg溶于1.4mL pH7.4的HEPES(10mmol/L)缓冲液中,再加入2mL 0.5% EDC,25℃反应8h,调节pH值至7.4,25℃反应4h。
反应物纯化后加入50μL的超纯水,25℃反应6h。用磁力搅拌器对反应液透析,透析3d。小分子物质被滤去。即形成无金属抗原BSA-GSH。
1.3.3 合成抗原的鉴定
1.3.3.1 蛋白质量浓度测定
将纯化后的抗原按照BCA蛋白检测试剂盒(DiacloneTM)说明书上的方法测定蛋白质量浓度。抗原的质量浓度测定以BSA作为标准蛋白,用BCA法构建质量浓度检测标准曲线。标准曲线的线性方程为:y=0.0013x-0.0015,线性相关系数为R2=0.9999,式中:y为样品在波长562nm处吸光度;x为样品蛋白质量浓度。
1.3.3.2 半抗原、抗原与载体蛋白的紫外光谱
以0.1mol/L、pH7.4 HEPES作为空白对照,取50μL BSA及其相应的抗原,用HEPES稀释至1mg/mL;取20μL半抗原,用HEPES稀释10倍,再用去离子水稀释5倍。在波长200~320nm范围内进行紫外扫描。
1.3.3.4 抗原中Hg2+含量的测定
以0.1mol/L、pH7.4的HEPES作为空白对照, 将离心纯化后的抗原用0.1mol/L、pH7.4 HEPES稀释100倍,参照国标GB/T 17141—1997《土壤质量 铅、镉的测定 石墨炉原子吸收分光光度法》,用石墨炉原子吸收光谱法检测抗原中Hg2+的浓度。
2 结果与分析
2.1 抗原中蛋白质量浓度的检测
利用BCA 法检测分离纯化后的Hg2+-GSH-BSA、 GSH-BSA中蛋白的质量浓度依次为(7.550±0.346)、(7.219±0.124)mg/mL(表1)。

表1 BCA法检测抗原中蛋白质量浓度Table 1 Carrier protein concentration in antigen determined by BCA method
2.2 紫外扫描定性分析
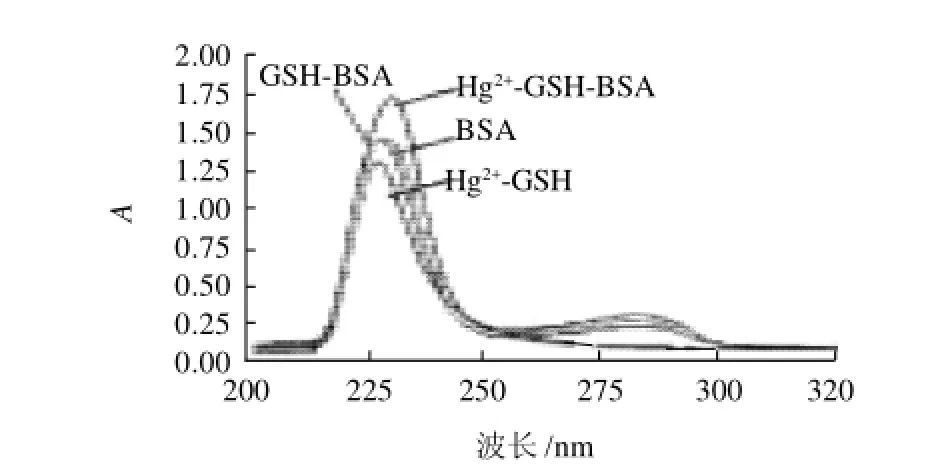
图1 紫外扫描载体蛋白和抗原的图谱Fig.1 UV scanning spectra of carrier protein and antigen
如图1 所示,BSA在波长227.5nm处和278nm处有一个吸收峰;半抗原BSA-GSH在波长218~235nm处有强吸收峰(吸光度均在0.5以上),属于高吸收值的区域;半抗原与载体蛋白相比,BSA-GSH的最大吸收波长发生了漂移,在波长218~235nm之间出现特征吸收峰。BSA-GSH-Hg2+在波长228.7nm处出现强吸收峰,在波长218~240nm之间出现高吸收值。结合以上信息,抗原BSA-GSH-Hg2+的紫外扫描特征既具有BSA的特征,又具有半抗原BSA-GSH的特征,证明抗原合成成功。
2.3 抗原SDS-PAGE电泳鉴定

图2 抗原SDS-PAGE电泳图Fig.2 SDS-PAGE of antigen
由图2可以看出,由于BSA上交联有螯合剂GSH,与BSA相比,分子质量变大,BSA-GSH电泳条带滞后且较模糊。同理BSA-GSH-Hg2+与BSA-GSH及BSA相比,分子质量变大,且由于Hg2+带正电,所以电泳条带滞后且模糊。由此可定性判断抗原合成成功。
2.4 石墨炉原子吸收光谱法检测抗原中Hg2+的含量
通过石墨炉原子吸收光谱法对产物Hg2+-GSH-BSA、GSH-BSA、HEPES中的Hg2+含量进行测定,其结果依次为:(206.4±0.7)、0、0μg/mL。进一步表明半抗原确实偶联到蛋白质上,证明抗原合成成功。
2.5 计算偶联比
通过计算,Hg的含量为1.029×10-6mol/mL;BSA的含量为0.1127×10-6mol/mL。Hg和BSA的偶联比为1.029:0.1127=9.131:1≈9:1。
3 结论与讨论
重金属离子免疫检测的关键在于重金属螯合物特异性单克隆抗体的制备,重金属螯合物特异性单克隆抗体制备的关键又在于重金属免疫原的制备。由于Hg2+能与动物体内生物分子发生强烈的不可逆反应,导致动物中毒,本实验选择了多氨基羧基化合物(谷胱甘肽)作为螯合剂,制备Hg2+人工抗原。
首先使谷胱甘肽和大分子蛋白结合形成大分子物质,再使谷胱甘肽上的二硫键和汞离子结合形成较稳定的复合体。汞离子此时就像一颗钻石镶嵌在大分子蛋白上,周围包裹汞离子的基团较少,这样使得汞离子获得一个空间表象,从而使得BSA-谷胱甘肽-汞离子的复合物具有较好的免疫原性和抗原反应性,可以使免疫系统间接对汞离子产生识别反应。
在免疫动物之前,需要对重金属抗原进行结构表征。本实验通过对抗原及相应载体蛋白的紫外光谱进行测定,并结合SDS-PAGE电泳结果,定性判定抗原合成是否成功。经鉴定合成成功的抗原,利用石墨炉原子吸收光谱法检测抗原中的Hg2+含量,并使用BCA试剂盒获得偶联载体蛋白的量,求得产物的偶联比率是9:1,该研究成果为重金属螯合物单克隆抗体的制备提供了参考。
[1] 常学秀, 文传浩, 王焕校, 等. 重金属污染与人体健康[J]. 云南环境科学, 2000, 19(1): 59-61.
[2] DIANE B, JONES R M, ROBERT C B, et al. Antibody-based sensors for heavy metal ions[J]. Biosen Bioelec, 2001, 16: 799-809.
[3] 王宏镇, 束文圣, 蓝崇饪. 重金属污染生态学研究现状与展望[J]. 生态学报, 2005, 25(3): 596-605.
[4] 夏立江, 华珞. 重金属污染生物修复机制及研究进展[J]. 核农学报, 1998, 1(12): 59-64.
[5] 金岚. 环境生态学[M]. 北京: 高等教育出版社, 1992: 232-238.
[6] 谢华林, 张萍, 贺惠, 等. 大气颗粒物中重金属元素在不同粒径上的形态分布[J]. 环境工程, 2002, 20(6): 55-58.
[7] NRIAGU J O. Changing metal cycles and human health[M]. Berlin: Sprintger-Verlog, 1984: 113-141.
[8] 庄树宏, 王克明. 城市大气重金属(Pb、Cd、Cu、Zn)污染及其在植物中的富积[J]. 烟台大学学报, 2000, 13(1): 31-37.
[9] 杨燕娜, 温小乐. 土壤汞污染及其治理措施的研究综述[J]. 能源与环境, 2006(3): 9-11.
[10] 刘功良, 王菊芳. 重金属离子的免疫检测研究进展[J]. 生物工程学报, 2006, 22(6): 877-881.
[11] 黄佳俊, 王菊芳, 刘功良, 等. 重金属汞鳌合物人工抗原的合成与鉴定[J]. 中国生物工程杂志, 2008, 28(2): 71-75.
[12] BLAKE II R C, DELEHANTY J B, KHOSRAVIANI M. Allosteric binding properties of a monoclonal antibody and its fab fragment[J]. Biochemistry, 2003, 42(2): 497-508.
[13] JOHANSON D K. A fluorescence polarization immunoassay for cadmium (II)[J]. Analytica Chimica Acta, 1999, 399(1/2): 161-172.
[14] KHOSRAVIANI M, PAVLOV A R, FLOWERS G C, et al. Detection of heavymetals by immunoassay: optimization and validation of a rapid, portable assay for ionic cadmium[J]. Environ Sci Technol, 1998, 32(1): 137-142.
Synthesis and Identification of Artificial Antigen for Mercury Chelate
JIANG Yun1,YAN Wen-jing2,LIU Li-qiang2,KUANG Hua2,CHEN Wei2,ZHANG Kun2,XU Chuan-lai2,*
(1. Analytical Center, Suzhou University, Suzhou 215123, China;2. School of Food Science and Technology, Jiangnan University, Wuxi 214122, China)
Mercury was used as the initial material to chelate GSH and obtain a bi-functional hepten of Hg-GSH chalete. The hapten was then coupled with the carrier protein such as bovine serum albumin (BSA) or ovalbumin (OVA) to obtain a complete antigen, Hg-GSH-BSA (OVA), whose successful synthesis was confirmed by ultra-violet spectrum and SDS-PAGE. On the basis of mercury content in synthesized products determined by atomic absorption spectrometry and the amount of carrier protein determined by bicinchoninic acid (BCA) assay, the coupling ratio between mercury and carrier protein calculated to be 9:1. The successful synthesis of Hg-GSH-BSA conjugate may lay a basis for preparing recognizing antibodies of mercury chelate.
mercury;heavy metal;immunoassay;bifunctional chelating agent;antigen
TS207.5
A
1002-6630(2011)07-0244-03
2010-07-16
蒋芸(1979—),女,实验师,硕士,研究方向为重金属残留检测。E-mail:jiangyun@suda.edu.cn
*通信作者:胥传来(1965—),男,教授,博士,研究方向为食品安全。E-mail:xcl@jiangnan.edu.cn



