李梦醒,王季石,张 燕,孙志强,赵 鹏,卢英豪
(贵阳医学院附属医院,贵州 550004)
慢性粒细胞白血病(chronic myeloid leukemia,CML)是一种获得性造血干细胞恶性克隆性疾病,CML患者中Ph(费城染色体)阳性率约为95%,疾病进入加速期(accelerated phase,AP)和急变期(blastic phase,BP)提示疾病进展,患者中位生存期2~12个月。甲磺酸伊马替尼(imatinib mesylate,IM 伊马替尼)是一种高度特异的酪氨酸激酶抑制剂,能抑制BCR/ABL酪氨酸激酶活性,使加速期和急变期患者生存时间明显延长[1]。对于移植后复发的患者,可以再次诱导使患者获得缓解[2],然而伊马替尼用于造血干细胞移植前后少有报道。因此,本研究回顾性分析了贵阳医学院附属医院血液科近年来进展期CML患者实行亲缘异基因造血干细胞移植(allogenetic hematopoietic stem cell transplantation,Allo-HSCT)联合伊马替尼治疗的结果。
1 资料与方法
1.1 一般资料 选取自2011年1月至2012年10月在贵阳医学院附属医院血液科住院病例中,采用Allo-HSCT联合甲磺酸伊马替尼治疗的进展期慢性粒细胞白血病共8例,6例急变期患者中5例为急性粒细胞白血病,1例为急性淋巴细胞白血病,所有病例经染色体及基因检测证实Ph染色体及BCR/ABL融合基因均阳性。患者及供者情况、HSCT前BCR/ABL融合基因见表1。8例供者均为亲缘供者,同胞供者5例,父母供者3例。
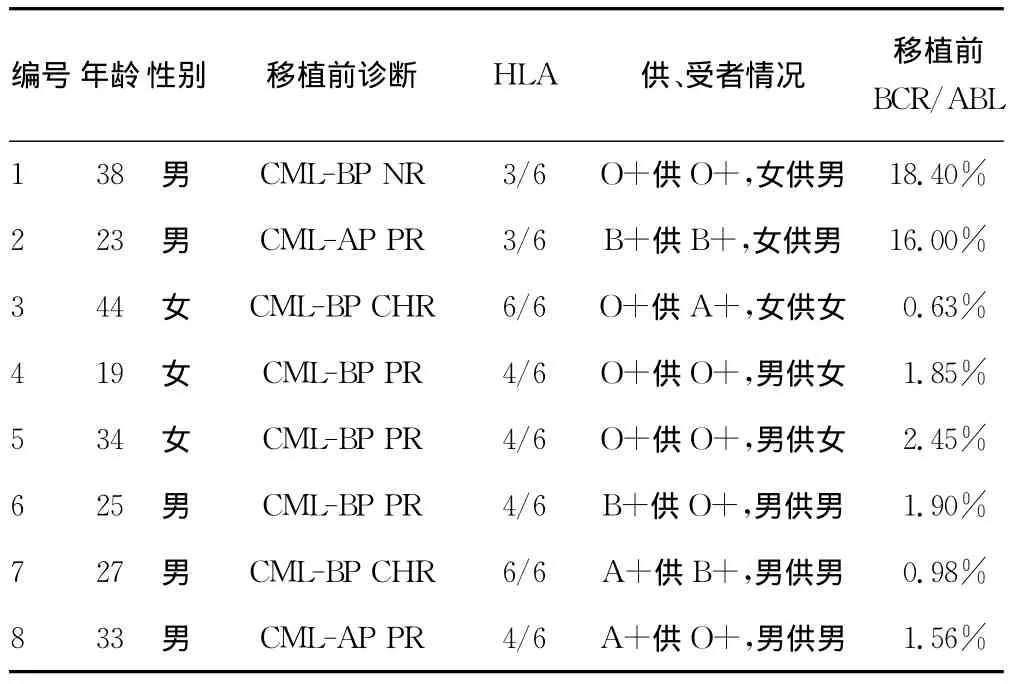
表1 供者、受者HSCT前BCR/ABL融合基因情况
1.2 方法
1.2.1 一般检测 供者、患者人类白细胞抗原(human leukocyte antigen,HAL)配型在贵阳医学院附属医院血液移植中心HLA配型室进行,实时定量PCR法进行BCR/ABL融合基因动态检测。
1.2.2 预处理方案 HLA全合采用改良Bu/CY方案:羟基脲80mg/(kg·d)×1d,阿糖胞苷(Ara-C):2g/(m2·d)×1 d,白消安(Bu)3.2mg/(kg·d)×3d,环磷酰胺(CTX)1.8g/(m2·d)×2d,甲基环基亚硝脲(Me-CCNU)250mg/(m2·d)×1d。HLA不合的采用改良Bu/CY方案联合ATG:Ara-C 4g/(m2·d)×2d,Bu 3.2mg/(kg·d)×3d,CTX 1.8g/(m2·d)×2d,Me-CCNU 250mg/(m2·d)×1d,3例患者加用VP-16。1例未缓解患者采用粒细胞集落刺激生长因子(GCSF)prime联合改良Bu/Cy及 ATG方案,G-CSF 5μg/(kg·d)×5d,Ara-C 3.0g/(m2·d)×3d;Bu 3.2mg/(kg·d)×3 d,CTX 1.8g/(m2·d)×2d,Me-CCNU 250mg/(m2·d)×1d。
1.2.3 干细胞动员及采集 干细胞动员采用G-CSF 5μg/(kg·d),皮下注射5~6d,骨髓及外周血干细胞采集及回输按照常规进行,所有患者均采用骨髓联合外周血干细胞移植。
1.2.4 移植物抗宿主病(graft-versus-host disease,GVHD)的预防 以环孢素A(CsA)、吗替麦考酚酯(MMF)加短程甲氨蝶呤(MTX)预防GVHD。
1.3 疗效评定标准及GVHD分度 以外周血中性粒细胞绝对值(ANC)≥0.5×109/L、血小板计数(PLT)≥20×109/L为造血功能重建标准。判断供者干细胞植入情况,不同性别检测受者移植后性染色体,相同性别检测移植前后供受者短串联重复(Short tandem repeat,STR),10个微卫星位点判断。GVHD按Fred Hutchinson标准进行各脏器分级及总分度[3]。随访至2012年10月15日。中位随访时间10.5个月(5~18个月)。
2 结 果
2.1 造血干细胞的植入情况 8例患者移植后均获得造血重建,中性粒细胞植活的中位时间为16d(12~22d),血小板植活的中位时间为18.5d(12~35d)。移植后1个月8例患者均获得不同程度的嵌合,6例获得完全嵌合(>95%),2例获得95%以下的混合嵌合,移植后2个月嵌合均达98%以上。
2.2 移植前后伊马替尼治疗结果 移植前经化疗联合伊马替尼治疗1例,达到部分缓解(PR),单用伊马替尼(格列卫)治疗的患者5例,其中2例达血液学完全缓解(CHR),3例PR。2例诱导化疗失败后,1例用伊马替尼挽救治疗达PR,1例未再进行其他治疗。移植后定期进行细胞形态学、嵌合度及融合基因定量检查,发现融合基因定量值进行性升高或嵌合度偏低,即给予伊马替尼早期干预治疗,伊马替尼的用量依据外周血三系变化情况及骨髓涂片检查其骨髓增生度而定。1例患者为慢粒急粒变未缓解,移植后28d嵌合体检测18.4%,BCR/ABL阳性,停用免疫抑制剂,加用伊马替尼治疗(400mg/d),59d后获得完全嵌合(98%)。2例患者移植后BCR/ABL定量进行性升高,移植后2月加用伊马替尼治疗(300mg/d),BCR/ABL转阴。4例移植后BCR/ABL未转阴患者均在移植后3个月开始服用伊马替(300~400mg/d),BCR/ABL转阴。1例患者移植后BCR/ABL阴性未服用伊马替尼。
2.3 GVHD的发生情况 8例异基因移植中,急性GVHD的发生率为75.0%(6/8),其中I度1例,Ⅱ度5例。8例患者存活均超过100d,慢性GVHD的发生87.5%,其中局限型5例,广泛型2例,主要累及皮肤、眼及肾。
2.4 其他并发症 出血性膀胱炎6例,巨细胞病毒(CMV)血症6例,细菌血行感染4例,继发三系减少1例,继发性癫痫1例,急性阑尾炎1例。
2.5 患者的存活及原发病复发情况 截至随访结束,6例患者无白血病存活(75.0%),多次行骨髓细胞形态学检查,维持完全缓解状态,BCR/ABL融合基因阴性,无病存活中位时间为8个月(7~17个月),随访期间死亡1例,复发1例,移植相关死亡率为12.5%。
3 讨 论
Ph即t(9;22)(q34;q11),以及与之相关的 BCR/ABL融合基因阳性。伊马替尼能够结合于ABL激酶域的非活化构象。从而阻断BCR/ABL激酶的活化,抑制白血病细胞的增殖[4],对Ph、BCR/ABL基因阳性的恶性血液病具有靶向治疗作用。
异基因干细胞移植是目前惟一有治愈CML可能的治疗方法,在慢性期(<1年)移植,5年生存率可达到40%~70% ,但对于加速期和急变期患者的疗效欠佳[5]。使用伊马替尼可使CML慢性期、加速期、急变期患者均有可能获得血液学和遗传学缓解[6],对于加速期和急变期患者,使用伊马替尼可以进行体内净化,减少肿瘤细胞负荷,使患者重新回到慢性期,延长了患者的存活时间,同时也为造血干细胞移植创造了更好的条件[7]。因此两者联合应用或许可以达到更好的治疗效果。Kukreja等[8]通过对HSCT前接受伊马替尼治疗治疗的白血病患者分析,得出移植前使用伊马替尼不增加移植相关毒性的结论,采用伊马替尼进行联合治疗可取得良好疗效。
本研究中,虽然移植前7例CML进展期患者在伊马替尼治疗2个月时获得了不同程度的血液学缓解,但均未获得遗传学完全缓解,说明进展期CML体内很少残留BCR/ABL阴性的正常造血干细胞,伊马替尼单用或联合化疗用于该类患者疗效欠佳,且疗效的持久性不肯定,因而应该及早行HSCT“抢先”治疗,可能改善移植效果,争取更多患者得到长期无病生存。移植过程中观察到伊马替尼未影响移植物植活,移植后BCR/ABL未转阴患者,移植后28~90d恢复使用伊马替尼,BCR/ABL融合基因分别在1~5个月转阴。1例CML-BP移植前未缓解病例,未使用伊马替尼,虽给予强预处理方案,但在移植后2周脾脏再次增大,1月嵌合状态低于50%。加用伊马替尼治疗后1月转为完全供者嵌合状态,脾脏缩小。另外1例患者移植后嵌合度88%,加用伊马替尼治疗后,嵌合度为98%。所以伊马替尼用于HSCT前可以降低患者体内肿瘤细胞负荷,为移植争取时间,移植后应用伊马替尼可以促进患者达到完全嵌合状态,清除肿瘤残留病灶,降低复发率。
目前,虽然造血干细胞移植被认为是可以治愈恶性血液病的方法,但是伊马替尼也有特有的优势,因此两者联合应用或许可以达到更好的治疗效果。由于本研究开展时间较短、病例数较少,其长期疗效仍有待更多的病例纳入研究和长时间观察。
[1]Jain P,Kantarjian H,Cortes J.Chronic myeloid leukemia:overview of new agents and comparative analysis[J].Curr Treat Options Oncol,2013,14(2):127-143.
[2]Luo Y,Lai XY,Tan YM,et al.Reduced-intensity allogeneic transplantation combined with imatinib mesylate for chronic myeloid leukemia in first chronic phase[J].Leukemia,2009,23(6):1171-1174.
[3]Ross WA,Couriel D.Colonic graft-versus-host disease[J].Curr Opin Gastroenterol,2005,21(1):64-69.
[4]Au WY,Caguioa PB,Chuah C,et al.Chronic myeloid leu-kemia in Asia[J].Int J Hematol,2009,89(1):14-23.
[5]Zhao Y,Liu L,Wang Y,et al.Efficacy and prognosis of chronic myeloid leukemia treated with imatinib mesylate in a Chinese population[J].Int J Hematol,2009,89(4):445-451.
[6]Palandri F,Castagnetti F,Alimena G,et al.The long-term durability of cytogenetic responses in patients with accelerated phase chronic myeloid leukemia treated with imatinib 600mg:the GIMEMA CML Working Party experience after a 7-year follow-up[J].Haematologica,2009,94(2):205-212.
[7]Oehler VG,Gooley T,Snyder DS,et al.The effects of imatinib mesylate treatment before allogeneic transplantation for chronic myeloid leukemia[J].Blood,2007,109(4):1782-1789.
[8]Kukreja M,Wang T,et al.Impact of prior imatinib mesylate on the outcome of hematopoietic cell transplantation for chronic myeloid leukemia[J].Blood,2008,112(8):3500-3507.



