周 志,范 刚,王可兴,莫开菊,程 超,潘思轶,*
(1.华中农业大学食品科学技术学院,湖北 武汉 430070;
2.湖北民族学院 生物资源保护与利用湖北省重点实验室,湖北 恩施 445000)
微波辅助酸解释放刺梨汁键合态香气物质的效果
周 志1,2,范 刚1,王可兴1,莫开菊2,程 超2,潘思轶1,*
(1.华中农业大学食品科学技术学院,湖北 武汉 430070;
2.湖北民族学院 生物资源保护与利用湖北省重点实验室,湖北 恩施 445000)
以野生刺梨汁为研究对象,采用微波辅助酸解,结合Amberlite XAD-2树脂吸附和GC-MS分析技术,研究其释放键合态香气物质的最佳微波辅助酸解条件,并与单一酸解比较其释放键合态香气物质的效果。结果表明:pH1.0含糖苷类物质的刺梨汁水相经800W功率的微波能辅助酸解3min后,再在40℃酸解36h,释放的键合态香气物质的种类最多;其中含量最高的是辛酸,其次为棕榈酸、4-(3-羟基-1-丁烯基)-3,5,5-三甲基-2-环己烯-1-酮、4-(5-羟基-2,6,6-三甲基-1-环己烯基)-3-丁烯-2-酮、2,4-二叔丁基苯酚等;微波辅助酸解释放刺梨汁键合态香气物质效果明显优于同pH值和同温度下酸解时间更长的单一酸解效果。
刺梨;键合态香气化合物;微波辅助酸解
刺梨(Rosa roxburghii Tratt.)系蔷薇科落叶灌木植物,别名山刺梨、赛哇(西藏)、野石榴(陕西)、刺果儿和蜂糖果(鄂西)等,多分布于海拔1000~1600m的山区和丘陵地带[1]。刺梨富含VC、SOD、VP等生物活性物质[2],其营养价值和药用价值极高,具有抗氧化、增强免疫、延缓衰老、抗肿瘤等多种生理作用[2-4]。
糖苷类物质(glycoside compounds)是植物体内的二级代谢产物,广泛存在于植物体的花、果实、根、叶等器官中,在叶子中由生物合成作用产生糖苷键合态的芳香前体,然后输送到花中,花开时通过植物体内源酶的酶解作用释放出各种芳香组分[5]。糖苷键合态香气物质(glycosidically bound aroma compound)是一类不具挥发性,常与水果中的糖类物质通过糖苷键结合,以糖苷形式存在的香气前体物质。这类物质在酸或酶的作用下水解释放出能被人们嗅觉感受到的被称为游离态香气物质(free aroma compounds,FAC)。早在1969年,Francis等[6]就对玫瑰花瓣中糖苷形式的单萜醇进行了研究,开辟了糖苷键合态香气物质研究的新领域。Stahl-Biskup等[7]阐述了与糖苷连接的挥发性化合物现状,并报道了150个植物种类中分布着脂肪醇、烷基酚和去甲基异戊二醇等糖苷配基近200种。
糖苷键合态香气物质释放出游离态香气物质的常用方法主要有酸法[8-10]或酶法[11-13]。目前,微波技术应用于天然活性物质的提取[14-16]已成为研究热点,且已应用于食品杀菌的生产实际中。夏涛等[17]研究认为微波浸提可提高茶叶中键合态糖苷类香气前体的浸出量。Bureau等[18]报道了微波辅助提取葡萄汁中的键合态香气物质具有简便和高效的特点。但将微波技术应用于刺梨汁键合态香气物质释放方面的研究尚无报道。本实验将微波技术与酸法相结合,研究其对刺梨汁键合态香气物质的释放效果,为今后微波杀菌技术应用于高品质果汁产品加工奠定一定的理论基础。
1 材料与方法
1.1 材料与试剂
野生鲜刺梨采于湖北省恩施市高山地带,采摘时间为9月中下旬。
环己酮(色谱纯) 美国Fluka公司;C8~C22正构烷烃(色谱纯) 美国Sigma公司;AmberliteXAD-2(20~60目) 美国Supelco公司;正戊烷、甲醇、乙醚、乙酸乙酯、盐酸、氢氧化钠、柠檬酸、磷酸氢二钠、无水硫酸钠均为分析纯。
1.2 仪器与设备
6890N/5975MSD气质联用仪 美国Agilent公司;SL280A型榨汁机 浙江苏泊尔炊具股份有限公司;TDL-5-A型离心机 上海安亭科学仪器厂;R-210型旋转蒸发器(带V-700 型真空泵) 瑞士B. chi公司;DW-86L626型超低温冰箱 青岛海尔特种电器有限公司;K.D浓缩器 广州精科仪器有限公司;DF-101S集热式恒温加热磁力搅拌器 郑州长城科工贸有限公司;P80D23N2L-A9型格兰仕微波炉 佛山市顺德区格兰仕微波炉电器有限公司。
1.3 方法
1.3.1 刺梨果汁的制备
新鲜刺梨果经挑选、洗净和切碎后用榨汁机压榨取汁。汁液经过滤、4500r/min离心15min后于-76℃超低温条件下冻藏,备用。
1.3.2 Amberlite XAD-2树脂处理
称取50g Amberlite XAD-2树脂置于索氏抽提器中,分别用甲醇、乙酸乙酯和戊烷各回流处理10h,然后浸入甲醇中备用。使用时将洗净的XAD-2树脂以甲醇为溶剂进行湿法装柱,用500mL蒸馏水洗柱(流速10mL/min)后备用。
1.3.3 刺梨汁中游离态和键合态香气成分的分离
冻藏刺梨原汁在3 0℃水浴条件下解冻,然后以3mL/min流速流经填充有Amberlite XAD-2树脂的柱子(Φ 2.2cm×50cm),接着用300mL去离子水洗柱以除去水溶性的糖、酸物质。再用300mL乙醚-戊烷(1:1,V/V)洗柱去除游离态挥发性物质,接着用300mL甲醇洗脱出吸附在树脂上的糖苷类物质,收集的甲醇部分在旋转蒸发器上减压浓缩(水浴温度32℃)至干,用30mL 0.06mol/L的柠檬酸-Na2HPO4缓冲液(pH 5.0)溶解,再用80mL乙醚-戊烷(1:1,V/V)分3次萃取以去除可能残存的游离态挥发性物质,获得的30mL水相备用。
1.3.4 微波辅助酸法释放刺梨汁键合态香气物质的单因素试验
将1.3.3节获得的30mL水相用1mol/L HCl溶液调整至一定pH值后,置于聚四氟乙烯管(Φ 26mm×20cm)中,密封,然后用800W微波辅助酸解一段时间,冷却,转入50mL顶空瓶密封后,于40℃水浴中继续酸解一段时间,将酸解结束后的样品冷却后用1mol/L NaOH溶液调pH值至中性,再用80mL乙醚-戊烷(1:1,V/V)分3次萃取酸解液,无水硫酸钠干燥,K.D浓缩器浓缩至15mL,N2浓缩至0.5mL,取1μL供气相色谱-质谱分析(gas chromatography-mass spectrometry,GC-MS)。各因素水平:微波处理时间1、2、3、4min,pH值为0.5、1、1.5、2、2.5、3、3.5、4,水浴处理时间12、2 4、36、4 8、6 0h。
1.3.5 键合态香气物质的微波辅助酸法释放的正交试验
在单因素试验的基础上,选取pH值、微波处理时间和水浴处理时间三因素,采用L9(34)正交设计,研究释放刺梨汁键合态香气物质的最佳微波辅助酸解条件。因素水平见表1。
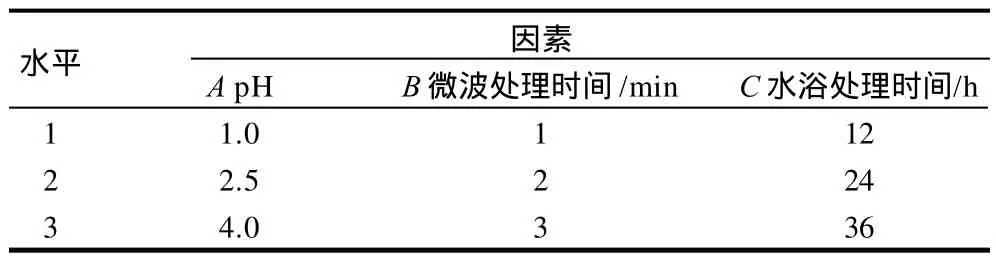
表1 微波辅助酸解因素和水平表Table1 Factors and levels of orthogonal array design
1.3.6 GC-MS分析条件
气相色谱条件:HP-5毛细管柱(30m×320μm,0.25μm);载气为氦气;进样口温度250℃;升温程序为起始温度40℃,保持3min,以4℃/min升温至220℃,再以10℃/min升温至250℃,保持5min。采用微量进样器进样,进样量分流比为1:20,溶剂延迟时间为6min。
质谱条件:色谱-质谱接口温度280℃,离子源温度230℃,四极杆温度150℃;离子化方式:EI;电子能量70eV;质量扫描范围45~550u。
1.3.7 挥发性成分的鉴定及定量
挥发性成分经过GC-MS分析鉴定后,其结果用计算机谱库(NIST 05/WILEY)进行检索及分析,并采用线性保留指数(retention index,RI)和质谱检索进行二维定性,结合相关的文献资料,确认挥发性物质的化学成分。
挥发性成分的含量采用内标法进行定量,内标物为环己酮。计算公式为:
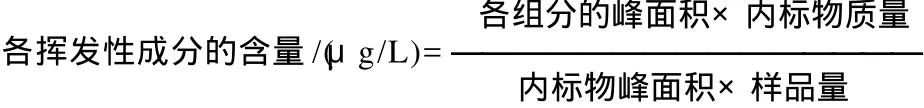
2 结果与分析
2.1 微波辅助酸解释放键合态香气物质的单因素试验
2.1.1 微波处理时间的选择
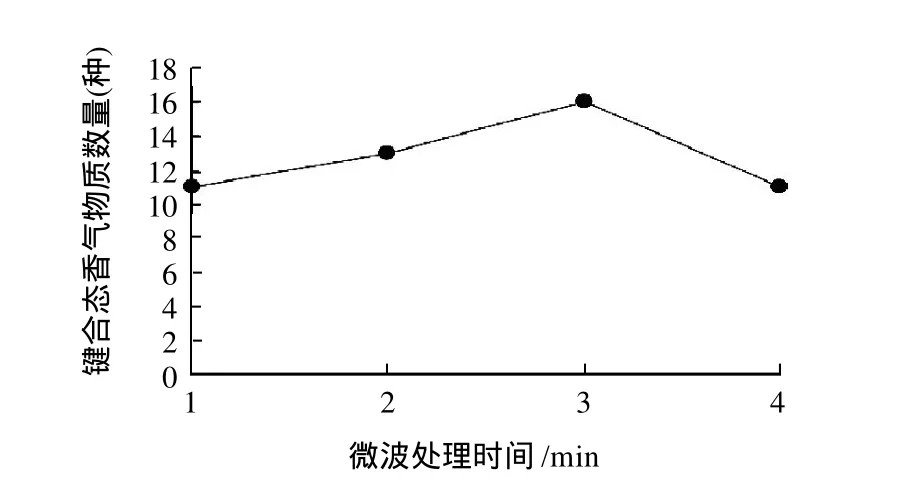
图1 微波处理时间对刺梨键合态香气物质的释放效果Fig.1 Effect of microwave treatment time on the release of bound volatile aroma compounds
孙爱东等[9]采用pH1.0、煮沸30min的酸解条件对甜橙中的糖苷键合态香气物质水解释放后发现,酸解能够释放较多的键合态组分。由图1可知,随微波处理时间的延长,释放键合态香气物质的数量越多;但当时间超过4min时,键合态香气物质的数量又有所下降。这主要是由于当前微波杀菌设备无反压控制装置,在实验或生产实践中当微波作用强度过强或微波作用时间过长时易出现胀袋或胀罐的现象,从而导致键合态香气物质的逸散。
2.1.2 pH值的选择
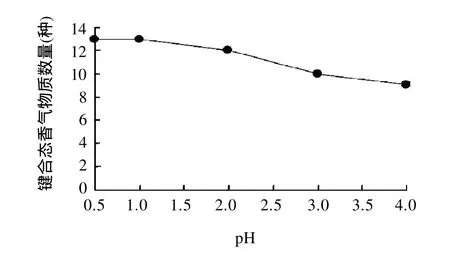
图2 pH值对刺梨键合态香气物质的释放效果Fig.2 Effect of hydrolysis pH on the release of bound volatile aroma compounds
图2表明,随着含刺梨糖苷类物质的水相pH值的增加,释放键合态香气物质的数量反而减少。这可能是较强的酸性环境更有利于键合态香气前体物质糖苷键的断裂。但刺梨汁的酸度过高,会影响刺梨产品的感官品质(主要是口感)。为了适应低酸低盐食品的消费趋势,通过降低pH值获得更多键合态香气物质的同时需保证产品口感。
2.1.3 水浴处理时间的选择
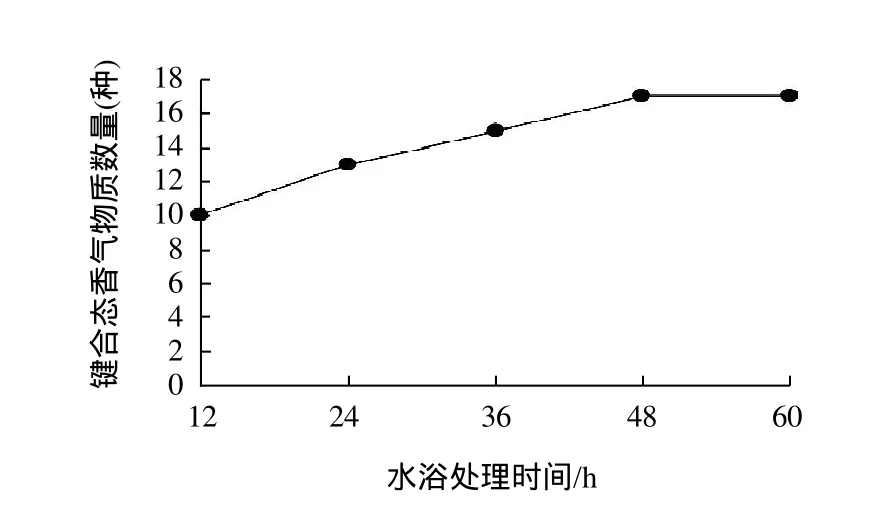
图3 水浴处理时间对刺梨键合态香气物质的释放效果Fig.3 Effect of water bath treatment time on the release of bound volatile aroma compounds
图3表明,随水浴处理时间的延长,释放键合态香气物质的数量越多,但当水浴处理时间超过48h时,键合态香气物质数量变化不大。
2.2 微波辅助酸解释放键合态香气物质条件优化
由表2可知,影响刺梨汁键合态香气物质释放效果因素的优先顺序为:微波处理时间>pH值=水浴处理时间。随着微波处理时间的延长,刺梨汁中产生键合态香气物质的种类逐渐增多;随着含有糖苷类物质水相pH值的逐渐增高,释放出的键合态香气物质的种类反而下降;随着40℃水浴处理时间越长,刺梨汁中释放出的键合态香气物质越丰富。因此,微波辅助酸解释放刺梨汁键合态香气物质条件的最佳组合为:A1B3C3,即pH1.0含糖苷类物质的水相经800W功率的微波能辅助酸解3min,再于40℃酸解36h。
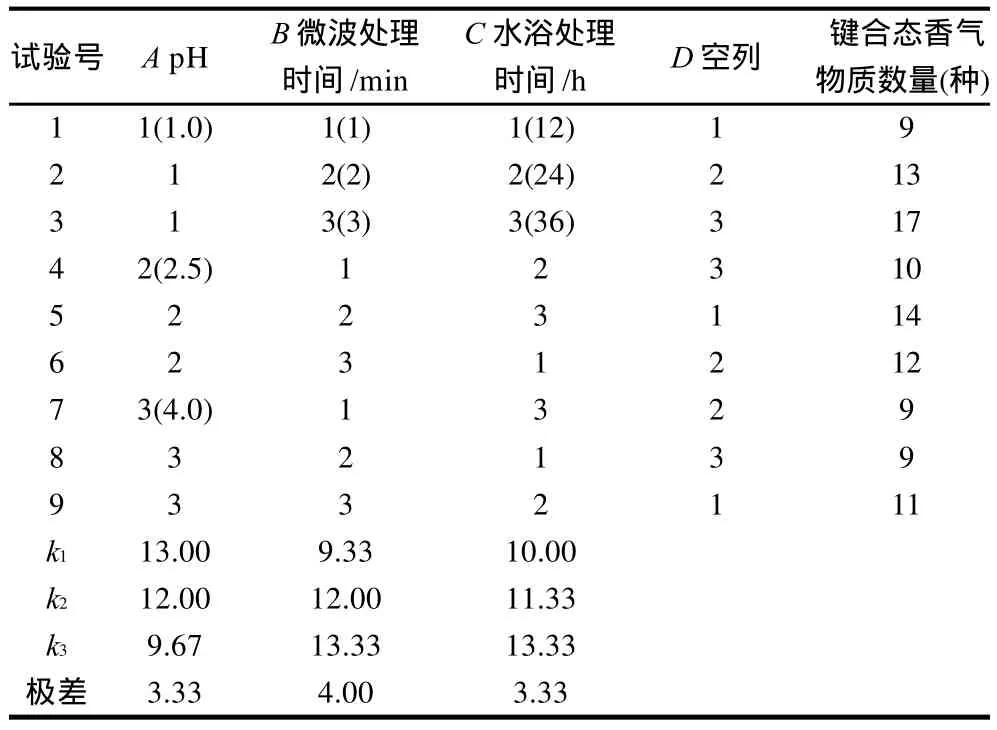
表2 微波辅助酸解释放键合态香气物质正交试验设计及结果Table 2 Orthogonal array design scheme and experimental results
2.3 微波辅助酸解与酸解释放键合态香气物质效果比较
采用最佳微波辅助酸解条件,对含糖苷类物质水相进行键合态香气物质释放的重复实验,并与pH1.0含糖苷类物质的水相在40℃直接酸解48h和96h进行比较,结果见表3。
由表3可知,微波辅助酸解和酸解均能促进刺梨汁键合态香气物质的释放,且微波辅助酸解对刺梨汁键合态香气物质的释放效果明显优于单一酸解的效果。去除游离态香气物质的刺梨汁水相,采用pH1.0、40℃酸解48h,可释放7种键合态香气物质;采用pH1.0、40℃酸解96h,可释放10种键合态香气物质;而采用pH1.0、微波3min结合40℃酸解36h,可释放17种键合态香气物质。这三种释放刺梨汁键合态香气物质的方式所释放的共同键合态香气物质有辛酸、4-(3-羟基-1-丁烯基)-3,5,5-三甲基-2-环己烯-1-酮和棕榈酸3种。微波辅助酸解释放出了一些单一酸解尚未释放出的如半乳糖酸内酯、赤藓糖醇和4-(5-羟基-2,6,6-三甲基-1-环己烯基)-3-丁烯-2-酮等风味增强剂。
pH1.0刺梨汁在40℃温度下酸解48h所释放的键合态香气物质中,含量最高的是4-(3-羟基-1-丁烯基)-3,5,5-三甲基-2-环己烯-1-酮(2771.9μg/L),其次为辛酸(471.2μg/L)、棕榈酸(283.9μg/L)、2-甲基间苯二酚(177.8μg/L)、3-羟基苯甲醇(38.4μg/L),含量最少的是2,5-二叔丁基苯酚(5.4μg/L)。pH1.0、40℃酸解96h所释放的键合态香气物质中,含量最高的是4-(3-羟基-1-丁烯基)-3,5,5-三甲基-2-环己烯-1-酮(3837.0μg/L),其次为棕榈酸(1810.2μg/L)、辛酸(1103.6μg/L)、2-(3-甲基苯氧基)乙醇(374.2μg/L)、2-羟基环十六烷酮(161.1μg/L)、3-羟基苯甲醇(118.5μg/L),含量最低的是2-甲基间苯二酚(13.3μg/L)。而pH1.0、微波3min结合40℃酸解36h所释放的键合态香气物质中,含量最高的是辛酸(4365.5 μg/L),其次为棕榈酸(2608.8μg/L)、4-(3-羟基-1-丁烯基)-3,5,5-三甲基-2-环己烯-1-酮(2442.4μg/L)、4-(5-羟基-2,6,6-三甲基-1-环己烯基)-3-丁烯-2-酮(695.6μg/L)、2,4-二叔丁基苯酚(400.9μg/L),含量最低的是α-无水葡萄糖酯(1.4μg/L)。
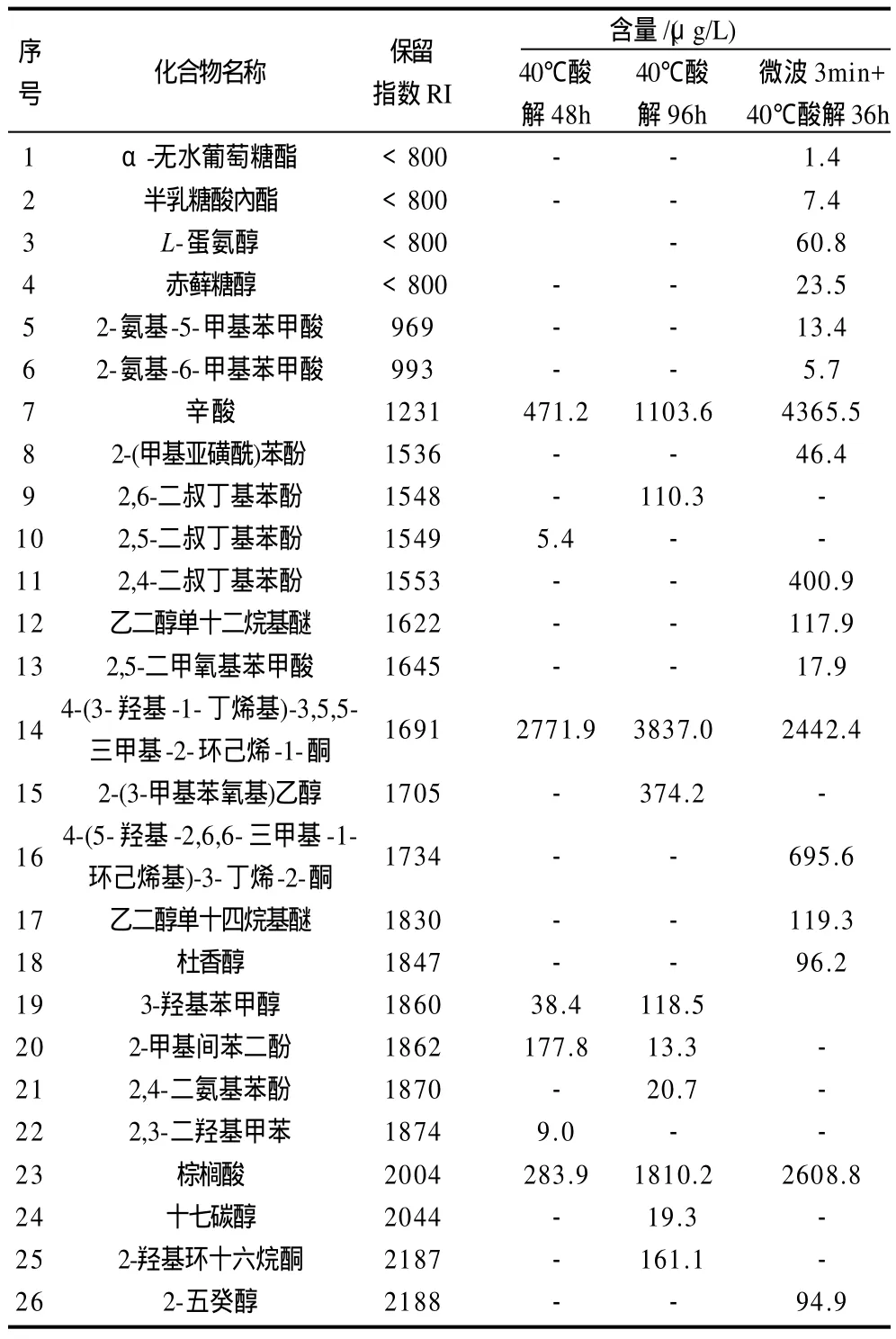
表3 不同水解方法水解出来的刺梨汁中键合态风味组分Table 3 Bound volatile aroma compounds of Cili pear juice as released by different hydrolysis methods
3 结论与讨论
微波辅助酸解释放刺梨汁键合态香气物质的最佳条件为:pH1.0含糖苷类物质的水相经800W功率的微波能辅助酸解3min后,再在40℃温度下酸解36h。最佳条件下的微波辅助酸解释放刺梨汁键合态香气物质效果明显优于同pH值同温度下酸解时间更长的单一酸解效果。pH1.0相同介质下,微波辅助酸解(微波3min结合40℃酸解36h)能释放17种键合态香气物质,而40℃单一酸解96h只能释放10种,40℃单一酸解48h释放仅有7种。
孙爱东等[9]采用pH1.0、煮沸30min的酸解条件对甜橙中的糖苷键合态香气物质水解释放后发现,酸解后的多数物质对橙汁的典型风味贡献不大。本研究嗅感分析表明,微波辅助酸解释放的刺梨汁挥发性香气较酸解释放的更浓郁,更愉悦,但其大多数挥发性香气物质对刺梨汁的天然风味贡献不大。Maicas等[19]研究发现含萜烯醇类配基的糖苷键合态香气物质经酸水解后,配基在酸性条件下可发生分子重排而转变为另一种物质。微波辅助酸水解和酸水解释放的香气组分大多不同,这可能与其水解机制和作用强度不同有关。随着微波辅助酸解机制的深入研究及其对释放香气物质的调控,将微波辅助酸解技术应用于提高果蔬制品的风味将具有广阔的应用前景。
[1] 刘孟军. 中国野生果树[M]. 北京: 中国农业出版社, 1998: 217-222.
[2] 方修贵, 李嗣彪, 郑益清. 刺梨的营养价值及其开发利用[J]. 食品工业科技, 2004, 25(1): 137-138.
[3] Van RENSBURG C J, ERASMUS E, TOIT D, et al. Rosa roxburghii supplementation in a controlled feeding study increases plasma antioxidant capacity and glutathione redox state[J]. Eur J Nutr, 2005, 44(7):452-457.
[4] ZHANG Chunni, LIU Xiaozhuan, QIANG Hongjuan, et al. Inhibitory effects of Rosa roxburghii Tratt juice on in vitro oxidative modification of low density lipoprotein and on the macrophage growth and cellular cholesteryl ester accumulation induced by oxidized low density lipoprotein[J]. Clin Chim Acta, 2001, 313(2): 37-43.
[5] WILLAMS P J, SEFTON M A, MARINOS V A. Recent developments in flavor and fragrance chemistry[C]//Proceedings of the Third International Haarman and Reimer Symposium in Tokyo. Tokyo, 1993: 283-290.
[6] FRANCIS M J O, ALLCOCK C. Geraniol β-D-glucoside occurrence and synthesis in rose flowers[J]. Phytochemistry, 1969, 8(8): 1339-1347.
[7] STAHL-BISKUP E, INTERT F, HOLTHUIJEZEN J, et al. Glycosidically bound volatiles: a review 1986-1991[J]. J Flavour and Fragrance,1993, 8(2): 61-80.
[8] GUNATA Y Z, BAYONOVE C, BAUMES R, et al. Stability of free and bound fractions of some aroma components of grape cv Muscat during the wine processing[J]. American Journal of Enology and Viticulture,1985, 37: 112-114.
[9] 孙爱东, 葛毅强, 阎红, 等. 甜橙键合态芳香组分的酶(酸)解解离方法研究[J]. 食品与发酵工业, 2000, 27(3): 33-36.
[10] 范刚, 张弛, 柴倩, 等. 锦橙汁键合态香气物质酸解和酶解效果比较研究[J]. 食品科学, 2007, 28(12): 169-172.
[11] GUNATA Z, BITTEUR S, BRILLOUET J M, et al. Sequential enzymic hydrolysis of potentially aromatic glycosides from grape[J]. Carbohydrate Research, 1988, 184: 139-149.
[12] 汤坚, 何其傥. β-葡甙酶水解法分析新鲜芹菜的游离态与糖甙键合态挥发性化合物[J]. 无锡轻工业学院学报, 1990, 9(4): 22-29.
[13] 孙爱东, 葛毅强, 倪元颖, 等. 不同来源的增香酶酶解橙汁(皮)中键合态主要芳香物质的效果分析[J]. 食品与发酵工业, 2001, 27(11):1-4.
[14] 汪兴平, 周志, 莫开菊, 等. 微波对茶多酚浸出及其结构和组成的影响研究[J]. 农业工程学报, 2002, 18(2): 110-114.
[15] SPIGNO G, De FAVERI D M. Microwave-assisted extraction of tea phenols: a phenomenological study[J]. Journal of Food Engineering,2009, 93(2): 210-217.
[16] WANG Sijin, CHEN Fang, WU Jihong, et al. Optimization of pectin extraction assisted by microwave from apple pomace using response surface methodology[J]. Journal of Food Engineering, 2007, 78(2): 693-700.
[17] 夏涛, 时思全, 宛晓春. 微波、超声波浸提对茶汤香气的影响[J]. 南京农业大学学报, 2004, 27(3): 99-102.
[18] BUREAU S, RAZUNGLES A, BAUMES R, et al. Glycosylated flavor precursor extraction by microwaves from grape juice and grapes[J]. Journal of Food Science, 1996, 61(3): 557-559.
[19] MAICAS S, MATEO J J. Hydrolysis of terpenyl glycosides in grape juice and other fruit juices: a review[J]. Applied Microbiology and Biotechnology, 2005, 67(3): 322-335.
Releasing Effect of Microwave-Assisted Acid Hydrolysis on Bound Volatile Aroma Compounds in Rosa roxburghii Tratt (Cili Pear) Juice
ZHOU Zhi1,2,FAN Gang1,WANG Ke-xing1,MO Kai-ju2,CHENG Chao2,PAN Si-yi1,*
(1. College of Food Science and Technology, Huazhong Agricultural University, Wuhan 430070, China;2. Key Laboratory of Biologic Resources Protection and Utilization of Hubei Province, Hubei Institute for Nationalities, Enshi 445000, China)
The bound volatile aroma compounds of wild Cili pear juice were extracted by chromatographic separation on an Amberlite XAD-2 column followed by microwave-assisted acid hydrolysis (acid hydrolysis first under microwave treatment and then in a 40 ℃ water bath) and analyzed by GC-MS. One-factor-at-a-time and orthogonal array design methods were used for the optimization of microwave-assisted acid hydrolysis conditions. The most types of bound volatile aroma compounds were extracted when the water phase fraction obtained from Amberlite XAD-2 column chromatographic separation was adjusted to pH 1 with 1 mol/L HCl solution, treated by microwave for 3 min at 800 W and then kept in a 40 ℃ water bath for 36 h.Octanoic acid was identified as the most abundant compound, followed by n-hexadecanoic acid, 4-(3-hydroxy-1-butenyl)-3,5,5-trimethyl-2-cyclohexen-1-one, 4-(5-hydroxy-2,6,6-trimethyl-1-cyclohexen-1-yl)-3-buten-2-one, 2,4-bis(1,1-dimethylethyl)-phenol, etc. Under the same conditions of pH and water bath temperature, microwave-assisted acid hydrolysis was more effective in releasing bound volatile aroma compounds from wild Cili pear juice than single acid hydrolysis for a longer time.
Rosa roxburghii Tratt;bound volatile aroma compounds;microwave-assisted acid hydrolysis
TS214.2
A
1002-6630(2012)08-099-05
2011-11-25
周志(1974—),男,副教授,博士研究生,研究方向为食品风味化学。E-mail:zhouzhi77716@163.com
*通信作者:潘思轶(1964—),男,教授,博士,研究方向为食品科学。E-mail:pansiyi@mail.hzau.edu.cn



